Casi Clinici [DISMETABOLISMO] Una “dolce” gravidanza: Come interpretare le alterazioni del metabolismo glucidico in gravidanza (2010) |  |
Sintesi clinica
La signora Valentina, 37 anni, giunge all’osservazione del dott. Rossi all’8a settimana di gestazione. La paziente riferisce familiarità positiva per diabete mellito tipo 2 e patologie cardiovascolari. Affetta da tiroidite di Hashimoto da circa 5 anni, null’altro di patologico degno di nota da segnalare. All’anamnesi ostetrica: due precedenti gravidanze, 11 e 9 anni addietro, esitate in parto eutocico e non complicate da diabete mellito gestazionale. Da allora, incremento ponderale di circa 15 kg in 4-5 anni (in atto altezza 165 cm, peso 78 kg, indice di massa corporea [BMI] 28,7 kg/m2).
Obbiettivi
-
Far conoscere i nuovi criteri diagnostici del diabete mellito gestazionale
-
Valorizzare l’importanza di un corretto regime alimentare in gravidanza
-
Far emergere l’utilità del follow-up post gravidanza nella diagnosi precoce di diabete mellito e della correzione dello stile di vita nella prevenzione della malattia
-
Incoraggiare l’allattamento materno nelle donne con diabete mellito pregestazionale o diabete mellito gestazionale
Domanda
È già possibile fare una diagnosi? È indicato eseguire l’emoglobina glicosilata (HbA1c)?
Risposta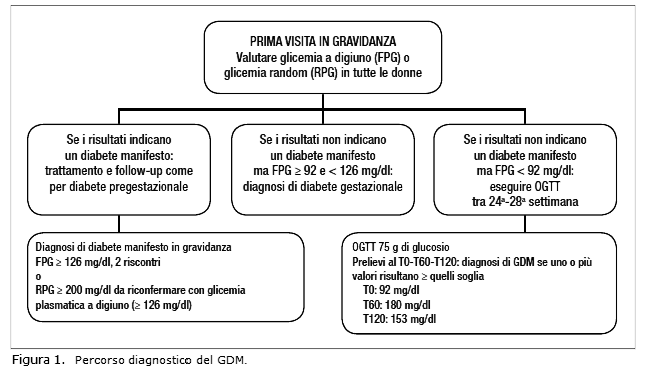
Secondo le recenti indicazioni del Gruppo di Studio AMD-SID (Associazione Medici Diabetologi - Società Italiana di Diabetologia) “Diabete e Gravidanza” 1, per porre diagnosi di diabete manifesto è necessario il riscontro ripetuto in due occasioni di un valore glicemico 126 mg/ dl. Tale diagnosi può avvenire anche mediante esecuzione di una glicemia random: il riscontro di un valore gli-cemico 200 mg/dl permette di dia-gnosticare un diabete manifesto, dopo conferma con glicemia plasmatica a di-giuno 126 mg/dl.
Non è attualmente indicato in gravianza il dosaggio dell’HbA1c ai fini diagnostici (Fig. 1).
Commento
I criteri diagnostici del diabete mellito gestazionale (GDM) sono stati recen-temente modificati alla luce dei risultati finali dello studio HAPO (Hyperglycemia and Adverse Pregnancy Outcome) 2 pubblicato nel maggio 2008 su The New England Journal of Medicine. Lo studio, condotto su oltre 25.000 gravide di varie etnie, ha evidenziato una relazione continua tra i livelli di glicemia materna registrati a digiuno e dopo 1 e 2 ore dal carico orale con 75 g di glucosio ed alterato outcome materno-fetale. Sulla base di questo studio, un panel internazionale di esperti (International Association of Diabetes and Pregnancy Study Groups, IADPSG) ha pubblicato pochi mesi fa le nuove proposte in materia di screening e diagnosi di GDM 3, ratificate successivamente dal Gruppo di Studio “Diabete e Gravidanza” AMD-SID, che ha preso in esame tale documento con l’obiettivo di adattare la realtà nazionale a queste indicazioni internazionali. Sulla base di ciò si è dunque stabilito che lo screening e la diagnosi di GDM debba avvenire in fase unica sostituendo il minicarico di glucosio con 50 g e la curva da carico con 100 g con un unico test da 75 g da effettuare tra la 24a e la 28a settimana di gestazione. Le soglie di normalità proposte sono di 92 mg/dl per la glicemia a digiuno, 180 mg/dl dopo un’ora e 153 mg/dl dopo 2 ore dal carico di glucosio. Si pone diagnosi di GDM quando uno o più valori risultano uguali o superiori a quelli soglia.
2° step
Il ginecologo richiede alla signora Valentina una nuova glicemia a digiuno riconvocandola a distanza di una settimana. Al secondo prelievo la glicemia risulta essere 125 mg/dl, pertanto viene inviata la gestante all’attenzione del diabetologo che programma un ulteriore dosaggio di glicemia plasmatica, determinata su campione di sangue venoso, da effettuare dopo almeno 8 ore di digiuno notturno. Viene chiesto al laboratorio di utilizzare, per la conservazione del campione, provette con sodio fluoruro, più idonee a questo tipo di misurazione poiché riducono la glicolisi e quindi la variabilità preanalitica del dosaggio della glicemia. Il dato che ne risulta è di 120 mg/dl, per cui il diabetologo pone diagnosi di diabete mellito gestazionale (non essendo stato confermato un valore ripetuto di glicemia # 126 mg/dl).
La signora Valentina, giunta all’11a settimana di gestazione, presenta un peso di 81 kg, altezza 165 cm, BMI 29,7 kg/m2, pressione arteriosa 110/65 mmHg. Riferisce di non fumare, né di bere alcolici e di praticare una leggera attività fisica (passeggiate quotidiane).
Effettuata la diagnosi, il team diabetologico imposta una terapia nutrizionale al fine di assicurare un’adeguata nutrizione materna e fetale, fornire un adeguato apporto calorico, garantendo un controllo glicemico ottimale senza determinare la comparsa di chetonuria. In gravidanza, infatti, non è raccomandata un’eccessiva riduzione calorica, in quanto la formazione di corpi chetonici conseguente al digiuno potrebbe risultare dannosa all’unità fetoplacentare.
La dieta viene personalizzata in relazione al BMI pregravidico secondo il seguente schema:
-
BMI < 18,5: 35 kcal/kg di peso corporeo pregravidico;
-
BMI 18,5-25: 30 kcal/kg di peso corporeo pregravidico;
-
BMI > 25: 24 kcal/kg di peso corporeo pregravidico.
A queste calorie, dal secondo trimestre di gravidanza viene aggiunto un supplemento per il feto di 300 kcal per le gestanti normopeso, 200 kcal per le pazienti sovrappeso. Viene dunque fornita alla paziente una dieta da 1850 kcal (la paziente rientra ancora al primo trimestre di gravidanza) suddividendo l’introito calorico complessivo in tre pasti principali e tre spuntini per meglio controllare le oscillazioni glicemiche proprie della gravidanza e ridurre le conseguenze legate al digiuno accelerato. Le kcal vengono suddivise secondo il seguente schema: prima colazione 10-15%; pranzo 20-30%; cena 30-40%; tre spuntini 5-10%. Il rapporto tra i diversi macronutrienti prevede il 45-50% di carboidrati, complessi e ricchi in fibra, il 20% di proteine, il 30-35% di lipidi.
Viene istruita la paziente all’automonitoraggio domiciliare della glicemia secondo uno schema a scacchiera e al controllo quotidiano della chetonuria al risveglio, consigliando inoltre di monitorare il peso corporeo una volta a settimana, preferibilmente nello stesso momento della giornata, con gli stessi indumenti e sulla stessa bilancia.
Commento
La gravidanza è caratterizzata dal fenomeno del “digiuno accelerato” dovuto a una continua sottrazione di glucosio da parte del feto, anche quando la gestante non ne assume con gli alimenti, e a un blocco nella dismissione degli aminoacidi gluconeogenetici; ciò comporta una maggiore tendenza alla chetosi da digiuno. Poiché diversi studi hanno dimostrato l’associazione esistente tra elevati livelli di chetoni e complicanze fetali, è importante istruire la paziente all’autocontrollo dei chetoni urinari da eseguire quotidianamente a digiuno sulle urine del mattino. Una chetonuria in questa fascia oraria, se non accompagnata da valori glicemici elevati, può infatti essere indicativa di un’assunzione insufficiente di carboidrati.
Domanda
È necessario dosare l’HbA1c?
Risposta
Pur non risultando utile ai fini diagnostici, il dosaggio dell’HbA1c, eseguito mensilmente, può invece integrare il dato dell’autocontrollo glicemico nel definire il grado di compenso metabolico raggiunto al fine di guidare i frequenti adeguamenti terapeutici necessari in corso di gravidanza. Va però considerato che i valori di normalità dell’HbA1c nella donna gravida sono inferiori rispetto a quelli riscontrati fuori dalla gravidanza, come dimostrato dallo studio HAPO 2; l’obiettivo da perseguire deve pertanto essere un valore inferiore al 6%.
3° step
Alla visita successiva (12a settimana di gestazione) la paziente presenta un peso corporeo stabile, chetonuria negativa e al diario glicemico una glicemia a digiuno frequentemente superiore a 95 mg/dl, valori post-pranzo e post-cena entro i limiti, ma valori di glicemia un’ora dopo colazione quasi costantemente superiori ai 140 mg/dl. Il valore di HbA1c è di 6,1%, l’esame delle urine nella norma. Viene pertanto prescritto un analogo rapido dell’insulina prima di colazione, al dosaggio di 6 UI/die, e insulina NPH 10 unità prima di coricarsi, entrambe da modificare in base al controllo glicemico giornaliero. Viene intensificato l’autocontrollo glicemico rimandando la paziente a una visita ambulatoriale a distanza di due settimane.
Domanda
Perché è importante l’autocontrollo domiciliare della glicemia?
Risposta
Numerose evidenze dimostrano come l’aumento della glicemia materna comporti un aumentato rischio di morbilità del feto e del neonato, e ciò è probabilmente la conseguenza dell’iperinsulinemia fetale indotta da un eccesso di glucosio materno. Il passaggio transplacentare di glucosio determina infatti iperglicemia fetale, iperinsulinemia compensatoria con conseguente eccessivo sviluppo dei tessuti insulino-sensibili e quindi macrosomia; inoltre, dopo resezione del cordone ombelicale, ipoglicemia neonatale. La riduzione del rischio di tali complicanze si ottiene attraverso la normalizzazione della glicemia materna che durante la gravidanza deve essere mantenuta entro i valori di 95 mg/dl a digiuno e 140 mg/dl un’ora dopo i pasti, secondo gli obiettivi indicati dall’American Diabetes Association (ADA) 4. A tale scopo risulta fondamentale che la gestante si attenga al regime dietetico prescritto e controlli a domicilio la glicemia capillare per eventuali modifiche terapeutiche da parte del team diabetologico.
4° step
A distanza di 2 settimane (14a settimana di gestazione) la signora Valentina presenta un peso di 81,3 kg e pressione arteriosa ambulatoriale di 100/60 mmHg. Al diario glicemico valori entro i limiti della norma, chetonuria negativa. La paziente riferisce di aver incrementato di 2 unità l’insulina serale per riscontro di più valori di glicemia a digiuno superiori a 95 mg/dl nel corso delle due settimane precedenti con miglioramento del compenso metabolico.
La valutazione biometrica a 14 settimane mostra una crescita fetale nella norma (circonferenza addominale al 55° percentile) e normale liquido amniotico. Essendo giunti al secondo trimestre di gravidanza, viene modificato il numero di kcal previste dalla dieta introducendo un supplemento per il feto di 200 kcal. Si rimanda pertanto la paziente a un controllo ambulatoriale a distanza di 2 settimane.
5° step
Nei mesi successivi la paziente si reca nell’ambulatorio di diabetologia con cadenza bisettimanale; alla 20a settimana di gestazione, per insorgenza di iperglicemia post-pranzo e post-cena, viene intensificato il trattamento insulinico prescrivendo uno schema a quattro iniezioni di insulina/die. La valutazione biometrica alla 22a settimana di gestazione mostra crescita e morfologia fetale nella norma.
L’ultima visita viene eseguita alla 37a settimana di gestazione: la signora Valentina pesa 87 kg, pressione arteriosa 100/55 mmHg, glicemie nella norma, chetonuria assente. L’ecografia ostetrica effettuata alla 35a settimana di gestazione mostra crescita fetale nella norma (circonferenza addominale al 60° percentile, peso fetale stimato 2550 g ± 10%).
Domanda
Cosa fare dopo il parto?
Risposta
Dal giorno del parto una donna con GDM dovrà sospendere l’eventuale trattamento insulinico praticato e proseguire il monitoraggio glicemico per i primi giorni successivi.
La tolleranza glucidica dovrà essere rivalutata mediante test di tolleranza a carico orale di glucosio (OGTT) (2 ore, 75 g) a distanza di 6-12 settimane dal parto 4.
In considerazione dell’elevato rischio di sviluppare diabete occorre raccomandare alla paziente di mantenere un corretto stile di vita e un peso corporeo nella norma, con un’alimentazione equilibrata e un’attività fisica regolare.
Commento
La gravidanza, con i suoi stravolgimenti metabolici, porta alla luce nelle donne affette da GDM un sottostante e silente rischio di sviluppare diabete mellito, contribuendo a identificare una popolazione su cui indirizzare strategie preventive. Queste pazienti dovrebbero essere arruolate in un programma di follow-up che consenta di prevenire o identificare precocemente un diabete mellito di tipo 2. A tal fine l’ADA suggerisce un programma, condiviso dal Gruppo di Studio “Diabete e Gravidanza” AMD-SID, che prevede l’esecuzione di una curva da carico di glucosio a 6-12 settimane dal parto 4. Se essa risulta normale, la paziente va rivalutata entro tre anni; se invece risulta alterata (alterata tolleranza al glucosio [IGT] e/o alterata glicemia a digiuno [IFG]) la paziente deve essere rivalutata dopo un anno In queste donne deve inoltre essere avviato un programma di intervento sullo stile di vita in grado di agire in maniera efficace su quelli che sono i fattori di rischio modificabili (sovrappeso, vita sedentaria, alimentazione non equilibrata, fumo, ipertensione e dislipidemia), importanti per l’eventuale successivo sviluppo di diabete di tipo 2.
Domanda
Una donna con GDM può allattare?
Risposta
Il diabete pregravidico e il GDM non rappresentano una controindicazione all’allattamento naturale, che, anzi, va incoraggiato anche nella paziente diabetica. Una recente revisione della letteratura 5 ha infatti evidenziato come l’allattamento materno non solo sia possibile in questa categoria di pazienti, ma rappresenti un fattore protettivo nei confronti dello sviluppo di diabete mellito 2, sia per la madre sia per il bambino, riducendo il rischio di sviluppare successivamente la malattia. Nelle donne che allattano, i bassi livelli di estrogeni potrebbero infatti indurre un effetto positivo sul metabolismo glucidico, riducendo di conseguenza il rischio di sviluppare diabete.
Bibliografia
-
Documento di consenso Gruppo di Studio SID-AMD “Diabete e Gravidanza”. http://www.siditalia.it/Documenti/Documento%20%20Finale%20Consensus%20Naz%20%20GDM_afterAM2.pdf
-
The HAPO Study Cooperative Research Group. Hyperglycemia and adverse pregnancy outcomes. N Engl J Med 2008;358:1991-2002.
-
International Association of Diabetes and Pregnancy Study Groups. Recommendations on the diagnosis and classification of hyperglycemia in pregnancy. International Association of Diabetes and Pregnancy Study Groups Consensus Panel. Diabetes Care 2010;33:676-82.
-
American Diabetes Association (ADA). Standards of medical care in diabetes. III. Detection and diagnosis of gestational diabetes mellitus (GDM). Diabetes Care 2008;31(Suppl.1):S15.
-
Taylor JS, Kacmar JE, Nothnagle M, et al. A systematic review of the literature associating breastfeeding with type 2 diabetes and gestational diabetes. J Am Coll Nutr 2005;24:320-6.



