Area Dolore – Cure Palliative [Numero 3 - Articolo 3. Giugno 2006] La gestione del dolore neuropatico: le evidenze basate sulla ricerca traslate nella pratica clinica |  |
Sintesi
Nella valutazione di un paziente con dolore cronico severo, la diagnosi gioca un ruolo significativo nella scelta del trattamento. Il dolore nocicettivo risponde bene ai FANS e agli oppiacei, mentre il dolore neuropatico generalmente non risponde ai FANS e spesso risponde solo ad alte dosi di oppiacei. La storia clinica è generalmente di aiuto nella diagnosi del dolore neuropatico. Spesso pazienti con dolore neuropatico riferiscono una sofferenza persistente o intermittente che è indipendente da uno specifico stimolo periferico. Il dolore persistente associato ad una neuropatia è descritto come simile ad una scossa elettrica, a un bruciore o a freddo gelido. Pazienti con danno al sistema nervoso periferico possono descrivere una spiacevole parestesia e disestesia (pizzicorio, puntura di spilli e/o aghi), formicolio ( la sensazione di un insetto che striscia sulla pelle) e/o intenso prurito. E comune per i pazienti descrivere più di un tipo di dolore. La diagnosi di dolore neuropatico è determinata dalla combinazione di disturbi sensitivi allesame obbiettivo e dal riscontro di danno al sistema nervoso. Lallodinia per il freddo e l iperalgesia sono comuni segni clinici nei pazienti con dolore neuropatico.
Meccanismi del dolore
Ci sono forti evidenze, tratte da modelli sperimentali su animali, che i sintomi del dolore neuropatico (iperalgesia per il calore e per gli stimoli meccanici, allodinia per il freddo e per gli stimoli meccanici ) hanno, almeno parzialmente, differenti meccanismi fisiopatologici e rispondono differentemente ai vari farmaci. Insieme questi risultati suggeriscono che il meccanismo che provoca il dolore neuropatico post-traumatico possa differire da quello responsabile del dolore neuropatico da chemioterapici. I ricercatori sono attualmente impegnati nella ricerca di evidenze cliniche per i differenti effetti farmacologici nelle varie risposte anomale del dolore.
Terapia centrata sui meccanismi fisiopatologici
Coerentemente con il concetto che diversi meccanismi fisiopatologici contribuiscono alla genesi del dolore neuropatico di varia etiologia, così come le risposte individuali al dolore, cè ampia evidenza clinica che le differenti sindromi di dolore neuropatico così come la neuropatia diabetica, la nevralgia post-erpetica e la nevralgia trigeminale rispondono differentemente alle diverse categorie di farmaci. Inoltre molti dati indicano che il dolore neuropatico derivi da un danno del nervo periferico o da modificazioni del sistema nervoso centrale che possono aumentare e sostenere la percezione del dolore indipendentemente dalla localizzazione o dalla causa del nervo danneggiato. Numerosi farmaci sono stati usati nel trattamento del dolore neuropatico. Gli antidepressivi triciclici, gli SNRIs duloxetina e venlafaxina e gli oppiacei influenzano le vie inibitorie discendenti del dolore. Altri farmaci hanno diversi meccanismi dazione e specificatamente: la modulazione dei canali del sodio ( carbamazepina, oxcarbazepina, lidocaina e gli antidepressivi triciclici ), inibizione dei canali del calcio voltaggio dipendenti (gabapentin, pregabalin ), il blocco dei recettori NMDA ( ketamina, destrometorfano ) e la stimolazione dei recettori alfa 2 adrenergici (tizanidina, clonidina ). Farmaci con differenti meccanismi dazione possono essere scelti in combinazioni basate su una potenziale sinergia.
Efficacia: dati clinici
Diversi farmaci si sono dimostrati efficaci nel trattamento del dolore neuropatico. Eguale efficacia nel dolore neuropatico è stata dimostrata in trials randomizzati e controllati dagli anestetici locali (cerotto di lidocaina al 5%, capsaicina ); dagli antiepilettici (gabapentin, valproato, carbamazepina, pregabalin ) dagli antidepressivi triciclici (nortriptilina e desipramina), dagli SNRIs (venlafexina e duloxetina, dagli oppiacei (ossicodone e tramadolo) e dagli agonisti dei recettori GABA-B ( baclofene ).
Gabapentin
Il gabapentin è un antiepilettico di seconda generazione con un meccanismo dazione sconosciuto, ma si pensa che agisca sui canali del calcio voltaggio dipendenti. Studi basati su modelli animale di dolore hanno dimostrato che gli effetti del gabapentin relativi al sollievo dal dolore neuropatico è mediato dalla inibizione del rilascio del glutammato nel corno dorsale del midollo spinale. Il gabapentin è approvato dalla FDA americana per il trattamento della nevralgia posterpetica (PHN). Lefficacia e la sicurezza del gabapentin nella riduzione del dolore posterpetico sono state esaminate in un trial di 8 settimane, multicentrico, randomizzato, in doppio cieco, in parallelo, contro placebo. Sono stati randomizzati un totale di 229 pazienti; 113 hanno ricevuto gabapentin e 116 placebo con il 79% e 82% di ogni gruppo, rispettivamente, che hanno completato lo studio. Alla fine dello studio 43.2% di quelli del gruppo del gabapentin, descrivevano il loro dolore come moderatamente o molto migliorato contro il 12.1% di quelli del gruppo placebo. La maggioranza dei pazienti che avevano ricevuto placebo ( 59.5%) non hanno sperimentato nessun cambiamento del loro livello di dolore, contro il solo 22.95 % di quelli che avevano preso il farmaco. Il numero di pazienti ritirati era simile tra i due gruppi, mentre sonnolenza, vertigini, atassia, edemi periferici, e infezioni erano nettamente più frequenti nel gruppo gabapentin. Complessivamente, il gabapentin è un farmaco sicuro ed efficace per il trattamento della nevralgia posterpetica. Il gabapentin tende ad avere meno effetti collaterali di molti antiepilettici di prima generazione e non ha nessuna significativa interazione farmacologia. Esso è raccomandato, in base alle evidenze cliniche, nella terapia del nevralgia posterpetica.
Analgesici topici
Parecchi anestetici locali, compreso la lidocaina, la capsaicina, e lEMLA (miscela di anestetici locali lidocaina al 25% e prilocaina al 25% ), sono stati studiati per luso nel dolore neuropatico. Sia la capsaicina in crema che i cerotti di lidocaina al 5% sono stati approvati dal FDA per luso nel trattamento della nevralgia posterpetica; è stata inoltre dimostrata lefficacia del cerotto di lidocaina al 5% nel trattamento del dolore delle neuropatie periferiche e per quanto riguarda la capsaicina nel trattamento della neuropatia diabetica dolorosa. La crema EMLA ha avuto un certo successo nel trattamento della nevralgia posterpetica in un piccolo numero di pazienti.
La Capsaicina, una sostanza irritante estratta dai peperoncini piccanti, depleta di sostanza P le fibre sensitive. Lefficacia di una crema di capsaicina al 0,025% è stata testata mediante una sperimentazione clinica controllata di 8 settimane con 39 pazienti con nevralgia posterpetica. I pazienti sono stati istruiti ad applicare la crema sulla zona dolorosa per 4 volte al giorno per tutta la durata dello studio.
Il principale risultatovalutabile era la riduzione del punteggio del dolore alla VAS. In 19 (48.7%) pazienti è stato notato un miglioramento; 5 pazienti hanno abbandonato lo studio (4 pazienti per il bruciore dopo lapplicazione della capsaicina e 1 per una mastite), 15 (38,5% ) non hanno avuto nessun miglioramento. Una riduzione statisticamente significativa del punteggio alla VAS era evidente dopo 2 settimane di applicazione continua. Unindagine di controllo condotta da 10 a 12 mesi dopo lo studio ha scoperto che 72.2% dei responders erano ancora migliorati. Un piccolo studio ha valutato gli effetti di una singola applicazione e di ripetute applicazioni di una crema di EMLA su 11 pazienti con nevralgia posterpetica. Dopo un periodo iniziale di una settimana, i pazienti hanno applicato della crema EMLA al 5% sullarea di maggior dolore con un bendaggio occlusivo per 5 ore al giorno per 6 giorni di fila. LEMLA non ha avuto alcun effetto significativo sul dolore spontaneo, sia dopo lapplicazione iniziale che 12 ore dopo lultima applicazione della serie. I pazienti hanno sperimentato una significativa riduzione del numero di attacchi dolorosi parossistici dal giorno dinizio sino al 7 giorno ( P < 0.001 ). Una singola applicazione della crema EMLA ha prodotto un effetto anestetico con un lieve sollievo del dolore e dellallodinia meccanica.
La lidocaina è un bloccante non specifico del canale del sodio che non può essere somministrato per bocca. Per esaminare gli effetti analgesici della lidocaina al 5% in cerotto è stato costruito uno studio in 4 sessioni, di 35 pazienti, randomizzato, in doppio cieco, comparato col cerotto vuoto. I pazienti arruolati nello studio presentavano una nevralgia posterpetica (PHN) con unarea cutanea ben individuata di allodinia sul dorso o agli arti. Ciascun paziente partecipava a 4 sessioni sperimentali di 12 ore: due in cui il cerotto di lidocaina al 5% era applicato sullarea di dolore più forte, una in cui si applicava il cerotto veicolo, e una senza alcun trattamento, sessione solamente di osservazione. I pazienti erano randomizzati per quanto riguarda lordine delle sessioni. Lintensità del dolore era misurata con una VAS a 100 mm. Comparato con la solo osservazione, il cerotto di lidocaina riduceva significativamente il punteggio del dolore per tutto il tempo ( da 30 minuti a 12 ore ); comparato con il solo veicolo, il cerotto di lidocaina riduceva significativamente il punteggio del dolore per il lintervallo tra la quarta e la dodicesima ora. Il cerotto veicolo era in grado di produrre un considerevole effetto placebo che svaniva entro le prime 4 ore di trattamento; leffetto del cerotto attivo rimaneva per tutta la durata della sessione ( 12 ore ). Recentemente è stato disegnato uno studio su larga scala con il cerotto di lidocaina al 5% per accertare la sua capacità di ridurre lintensità del dolore e linterferenza con la qualità di vita nei pazienti con PHN. I pazienti ( n=332 ) venivano istruiti ad applicare tre cerotti sullarea di maggior dolore per 12 ore al giorno per 28 giorni. Le valutazioni globali dei medici e dei pazienti dallinizio alla fine dello studio erano molto simili. Entrambe le valutazioni indicavano che circa il 60% di pazienti aveva avuto un completo o modesto miglioramento al 28° giorno. Approssimativamente il 20% di pazienti non sperimentarono nessun cambiamento in accordo con entrambe le valutazioni. In generale i trattamenti topici per il dolore neuropatico hanno un rischio minimo di effetti collaterali e di interazioni farmacologiche. La capsaicina è molto irritante. Il suo più comune effetto collaterale è una sensazione di bruciore che può essere lieve ma anche molto fastidiosa. La crema EMLA produce unanestesia locale con la sensazione di pelle intirizzita. Il più comune effetto collaterale dellEMLA è una reazione cutanea localizzata . Il cerotto di Lidocaina al 5%, produce un effetto analgesico locale, senza intirizzire la pelle. Anche per la lidocaina il più comune effetto collaterale è costituito da una reazione cutanea localizzata. Sia il cerotto di lidocaina che la capsaicina in crema sono raccomandati per il trattamento della nevralgia posterpetica, sebbene le evidenze di efficacia disponibili siano più forti per il cerotto di lidocaina che dimostra anche un uso più agevole.
Analgesici oppioidi
Gli oppioidi sono efficaci nel trattamento di alcuni tipi di dolore neuropatico così come del dolore nocicettivo. Alcuni studi clinici controllati contro placebo hanno mostrato che lossicodone, il tramadolo, il fentanyl e la morfina sono efficaci nel trattamento di alcune malattie dolorose neuropatiche. Il tramadolo è un analgesico sintetico ad azione centrale che agisce verosimilmente sia con i meccanismi monoaminergici che oppioidi. E un debole antagonista dei recettori oppioidi e ha proprietà agoniste sulla serotonina e noradrenalina. La sicurezza e lefficacia del tramadolo nella neuropatia diabetica dolorosa è stata esaminata tramite uno studio di 131 pazienti in doppio cieco, randomizzato, in parallelo, confrontato col placebo. Il dosaggio medio di tramadolo somministrato era di 210 mg/die. Alla valutazione finale, i pazienti che avevano ricevuto il tramadolo riportavano un significativamente più basso punteggio dellintensità del dolore di quelli che avevano ricevuto il placebo ( P < 0,001 ). Lossicodone è un potente analgesico oppioide di origine semisintetica, che come gli altri analgesici oppioidi è altamente efficace per il trattamento del dolore nocicettivo. Per stabilire lefficacia degli oppiacei nella gestione del dolore neuropatico è stato disegnato uno studio crossover, in doppio cieco in cui 50 pazienti con PHN sono stati randomizzati a ricevere 10 mg di ossicodone a rilascio controllato (CR) o placebo ogni 12 ore per 4 settimane. La dose è stata titolata settimanalmente sino ad un dosaggio di 30 mg/12 h. Hanno completato lo studio 38 pazienti. Il 67% dei pazienti identificarono il periodo del trattamento con ossicodone come il periodo preferito, in confronto del 11% che aveva preferito il placebo e il 22% che non aveva mostrato preferenze. Eeffetti collaterali degli oppioidi sono rappresentati da nausea, vomito, stipsi, sonnolenza e disturbi cognitivi, prurito, effetti neuroendocrini ( riduzione del testosterone ) e depressione respiratoria. La nausea e il vomito possono essere controllati con un antiemetico, e generalmente si sviluppa una tolleranza alla sonnolenza e ai disturbi cognitivi. Il prurito può essere risolto semplicemente con la rotazione degli oppiacei e la depressione respiratoria si vede più spesso in ambiente ospedaliero durante la gestione del dolore acuto. Le evidenze disponibili sostengono luso degli oppiacei orali a lunga azione e il tramadolo per il trattamento di alcuni tipi di dolore neuropatico.
Antidepressivi
Gli antidepressivi usati nella gestione del dolore neuropatico agiscono con diversi meccanismi dazione. Gli antidepressivi triciclici, considerati farmaci di primo impiego nel trattamento del dolore neuropatico, si crede influenzino le vie discendenti del dolore tramite linibizione della ricaptazione della serotonina e noradrenalina, unaffinità per il recettore H1 dellistamina, e un effetto sui canali del sodio. I triciclici con unattività SNRI (amitriptilina, nortriptilina, desipramina), sono particolarmente efficaci sul dolore neuropatico. Molti studi sono stati eseguiti sull uso dei triciclici nel trattamento delle neuropatie diabetiche e di altre neuropatie dolorose. Gli SNRIs (venlafexina e duloxetina) inibiscono in modo bilanciato la ricaptazione della serotonina e della noradrenalina, senza coinvolgere gli altri neurorecettori tipicamente coinvolti nella produzione degli effetti collaterali associati ai triciclici. La duloxetina è stata approvata dalla FDA per il trattamento della neuropatia diabetica . Le evidenze cliniche sullefficacia degli SSRIs sul dolore neuropatico sono inconsistenti. Gli antidepressivi costituiscono una scelta logica per il trattamento dei pazienti con dolore neuropatico non solo per la loro efficacia, ma anche perché al dolore si associa comunemente una depressione clinicamente significativa. Le evidenze mostrano la superiorità dei triciclici e degli SNRIs sui SSRIs nel conseguire la remissione dalla depressione. La frequenza di remissioni provenienti da 8 studi randomizzati, in doppio cieco sulla venlafaxina e gli SSRIs nel trattamento della depressione maggiore è stata comparata in un insieme di analisi. Le analisi includevano dati di 2.045 pazienti con depressione: tra questi, 851 erano trattati con venlafaxina a rilascio immediato e prolungato, 748 erano trattati con SSRIs e 446 erano in trattamento con placebo. I pazienti trattati con venlafaxina hanno avuto una frequenza di remissioni del 45% contro una frequenza di remissione del 35% e 25%, rispettivamente, con gli SSRIs e il placebo. Le differenze tra i gruppi erano statisticamente significative ( P < 0.001 per tutte le comparazioni ). Con luso accurato, esiste una considerevole e diffusa sicurezza e affidabilità dei triciclici. A causa della loro potenziale capacità di interagire con unampia varietà di recettori post-sinaptici, il loro uso può dare effetti collaterali di tipo colinergico ( secchezza delle fauci, visione doppia, stipsi ) alfadrenergico ( ipotensione, disfunzione sessuale, aumento di peso) istaminergico ( sedazione ). Bisogna avere la prudenza di evitarne luso nei pazienti più anziani. Si dovrebbe dare la preferenza agli agenti triciclici di seconda generazione ( nortriptilina e desipramina ) per i loro minor effetti collaterali, mentre lamitriptilina dovrebbe essere evitata nei pazienti più anziani.
Sommario
Unanalisi comparativa del NNT ( numbers-needed-to-treat ) per i più comuni farmaci usati nel dolore neuropatico mostra una frequenza di efficacia simile. Per la lidocaina in cerotto al 5% nelle sindromi da dolore neuropatico periferico il NNT era di 4.4. In uno studio sul trattamento della nevralgia post-erpetica i triciclici avevano un NNT di 4.0; per gli analgesici oppiacei era calcolato un NNT di 2.7. Due studi sul gabapentin nel trattamento della nevralgia posterpetica hanno ottenuto un NNT di 3.2 e 5.0 . La capsaicina ha ottenuto un NNt di 5.3 in uno studio sul trattamento della nevralgia poste-erpetica e 5.9 in studi sulla neuropatia dolorosa. In tutti i casi il NNT è stato calcolato utilizzando il criterio della riduzione del dolore di almeno il 50% alla fine del periodo di trattamento. In una meta-analisi di antidepressivi e anticonvulsivanti per la neuropatia diabetica e la nevralgia post-erpetica è stato calcolato il rapporto beneficio/danno per le varie categorie di farmaci esaminati. Per i più importanti effetti collaterali, gli antidepressivi in generale hanno un rapporto beneficio/danno di 6 ( p.es. ogni 6 pazienti che avranno un sollievo dal dolore >50%, 1 ridurrà il trattamento a causa degli effetti collaterali). Il rapporto beneficio/danno degli SSRIs e dei triciclici era rispettivamente 3 e 4. Gli antiepilettici hanno un rapporto beneficio/danno di 8 ( il gabapentin, 6; fenitoina e carbamazepina, 9 ). I farmaci di uso topico sono generalmente meno preoccupanti per il loro basso rischio di effetti sistemici. Il bruciore associato allapplicazione topica di capsaicina è spesso intollerabile. Sebbene le reazioni cutanee locali associate alluso della del cerotto di lidocaina al 5% siano molto comuni, tuttavia il cerotto è generalmente ben tollerato. Gli effetti collaterali degli oppiacei sono ben conosciuti e ben gestibili in molti casi, come discusso in precedenza.
Algoritmo per la scelta della terapia
Poiché il dolore neuropatico determina diversi sintomi, espressione spesso di molteplici meccanismi fisopatologici, cè da aspettarsi un effetto parziale come risultato di un trattamento con un singolo farmaco. Lutilizzo di più agenti con differente meccanismo dazione, sia della stessa che di diversa classe di farmaci può essere di sostanziale beneficio ai pazienti con dolore neuropatico. In altre parole, la gestione del dolore neuropatico è ben impostata con luso di una razionale associazione di farmaci. Nella seguente tabella sono delineati i principi di una razionale politerapia.
Tabella 1: Dieci principi per una razionale politerapia
- Dai priorità alla sicurezza e alla manegevolezza nel trattare il dolore cronico benigno.
- Dai priorità allefficacia nel trattare un paziente terminale con dolore.
- Esamina le potenziali interazioni con gli altri farmaci e con le condizioni cliniche.
- Preferisci selettivamente i farmaci per il dolore e per la concomitante depressione basandoti sullefficacia e sulla conoscenza dei meccanismi dazione.
- Confronta il peso degli effetti collaterali e del rischio di tossicità con lefficacia.
- Considera gli effetti farmacologici e lefficacia di altri analgesici.
- Considera gli effetti farmcologici sulle funzioni neuropsichiche quali umore, concentrazione, sedazione e memoria.
- Seleziona appropriate combinazioni di farmaci di differenti classi per ottenere lefficacia.
- Stabilisci un attendibile monitoraggio del dolore, dei livelli di attività ed altri indicatori di efficienza.
- Evita associazioni farmacologiche irrazionali.
Algoritmo per la scelta dei farmaci nel dolore cronico associato o meno a depressione
Un algoritmo per la scelta dei farmaci per il dolore cronico è illustrata nella figura 1 Come evidenziato più sopra, diversi farmaci sono disponibili per il trattamento del dolore neuropatico. Coesistenza di malattie mediche e psichiatriche così come potenziali rischi devono essere presi in considerazione nella scelta di una strategia di trattamento. Naturalmente la terapia medica può non essere la sola componente di un approccio multidimensionale di trattamento. In modo ottimale, il trattamento del dolore dovrebbe essere inserito in un rapporto di fiducia medico-paziente che coinvolga il paziente nella descrizione e nella condivisione degli obiettivi che il medico intende perseguire.
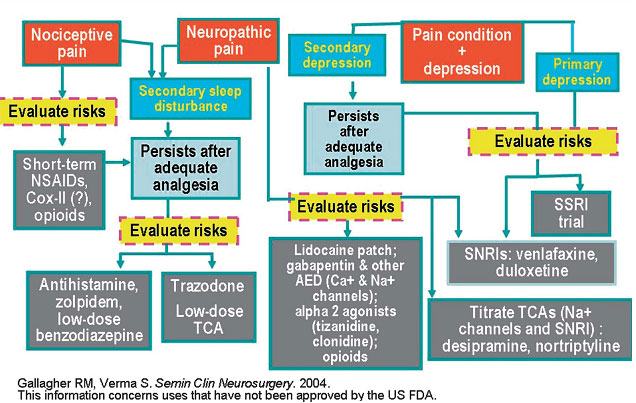
Legenda
- Evaluate risks: valutare eventuali controindicazioni e interazioni
- NSAIDs: FANS
- Cox-II: inibitori della Ciclossigenasi II
- TCA: antidepressivi triciclici
- Lidocaina patch: cerotto di lidocaina al 5% ( in Italia è in commercio la crema al 5% )
- Gabapentin & other AED: antiepilettici che agiscono sui canali del Na+ e Ca + ( Carbamazepina e oxcarbamazepina )
- Alpha 2 agonists: alfa 2 agonisti adrenergici ( Tizanidina e Clonidina )
- SSRI: inibitori selettivi del reuptake della serotonina
- SNRIs: inibitori selettivi del reuptake della noradrenalina e della serotonina
- TCAs: gli antidepressivi triciclici ( desipramina e nortriptilina ) che agiscono sui canali del sodio come gli SNRI
La percezione del dolore comporta una complessa interazione tra i sistemi neurofisiologici e comportamentali determinando o peggiorando una comorbidità psichiatrica. Il dolore persistente che non viene trattato, causa menomazioni e disabilità e può aggravare uneventuale comorbidità psichica e medica. La scelta di una terapia farmacologia deve prendere in considerazione laccertamento diagnostico, lefficacia, i meccanismi del dolore, il peso degli effetti collaterali, il rischio di tossicità, la sinergia, la facilità duso, ed i costi dei singoli farmaci. Possono essere necessari più farmaci che possano associare i loro effetti complementari. La gestione dei farmaci è incentrata su un completo piano gestionale centrato sul sollievo dal dolore e su obbiettivi di funzionalità.
Rilevanza per la Medicina Generale
Tre sono i punti di forza di questo articolo.
- Il richiamo forte ad una precisa diagnosi: prima di ogni scelta terapeutica è necessario classificare il tipo di dolore
- La diagnosi relativa alla presenza di una componente neuropatica: essa è essenzialmente clinica, ma si deve avvalere di conferme che derivano dallesame obiettivo ricercando i classici segni di neuropatia (iperlagesia, iperpatia, allodinia).
- La puntuale descrizione dei meccanismi fisiopatologici del dolore neuropatico e lesauriente panoramica dei farmaci attualmente disponibili per il trattamento di questo severo e non raro disturbo.
Nellambito della Medicina Generale la gestione del dolore neuropatico si presenta ancora come unarea di notevole criticità. Da un lato la componente neuropatica viene identificata con scarsa accuratezza diagnostica e dallaltro vi è il rischio di prescrizioni non appropriate dettate dalla pressione delle Aziende del farmaco e/o dai suggerimenti di Medici Specialisti. Lanalisi puntuale delle evidenze scientifiche in questo campo rappresentano la base perché esse possano trovare pratica e appropriata applicazione.
Commento del revisore
Larticolo può essere di ausilio per il medico di medicina generale nella gestione dei pazienti affetti da dolore neuropatico sia quando si imposti personalmente la terapia sia quando questa sia stata prescritta dagli specialisti del dolore. Di sicuro interesse gli studi sulla terapia topica con anestetici locali scarsamente conosciuta e ancor meno praticata negli ambulatori del MMG. In particolare luso del cerotto di lidocaina, per i suoi scarsi effetti collaterali e per i risultati riportati dagli studi clinici dovrebbe essere preso in seria considerazione dal medico di medicina generale nel trattamento della nevralgia posterpetica. Non sono state evidenziate, invece, dallautore dellarticolo le problematiche relative alluso degli anticonvulsivanti, in particolare del gabapentin, che pur essendo sicuramente efficace nel dolore neuropatico, presenta nella pratica clinica della medicina generale, un



